Nach einem Schnitt in den Finger kommen die Blutplättchen ins Spiel: Sie heften sich aneinander und verschließen auf diese Weise die Wunde. Eine wichtige Rolle bei diesem lebenswichtigen Mechanismus spielt der Adenosindiphosphat-Rezeptor P2Y12, der sich auf der Oberfläche der Blutplättchen befindet. Er gehört zur Familie der sogenannten G-Protein-gekoppelten Rezeptoren („GPCR“), für deren Erforschung im Jahr 2012 der Nobelpreis an zwei US-amerikanische Forscher verliehen wurde. „Dockt Adenosindiphosphat (ADP) als Bindungspartner an den Rezeptor an, werden Signale in das Zellinnere weitergeleitet, was schließlich zum Verklumpen der Blutplättchen führt“, sagt Prof. Dr. Christa Müller vom Pharma-Zentrum der Universität Bonn. Dabei passen der Rezeptor und der andockende Bindungspartner genau wie Schlüssel und Schloss zusammen. „Man kann sich das so vorstellen, dass das ADP wie ein Schlüssel den Rezeptor als Schloss aufschließt, um das Signal für die Verklumpung der Blutplättchen durchzulassen“, erläutert die Pharmazeutin.
Bessere Dosierung durch reversible Blockade
Manchmal ist die Blutgerinnung jedoch unerwünscht. So verstopfen zum Beispiel bei einem Herzinfarkt oder einem Schlaganfall die verklumpten Blutplättchen wichtige Gefäße. Zur Prophylaxe werden bei solchen Patienten meist Blutverdünner verschrieben, um weitere Schäden durch verschlossene Blutgefäße zu verhindern. Große Bedeutung haben Medikamente mit dem Wirkstoff Clopidogrel, der zunächst in der Leber aktiviert werden muss, dann den P2Y12-Rezeptor irreversibel blockiert und damit die Blutgerinnung verhindert. Durch die Bildung neuer Blutplättchen klingt dieser Effekt nach rund ein bis zwei Wochen in den Patienten wieder ab.
„Wünschenswert wäre eine wirksame, direkte, reversible Blockade des Rezeptors, um die Gerinnung besser steuern und Überdosierung verhindern zu können“, sagt Prof. Müller. Auch wenn ein mit Clopidogrel behandelter Patient einen Unfall erleidet, wäre ein Wirkstoff von Vorteil, der sich vom Rezeptor wieder lösen ließe. Das würde verhindern, dass der verletzte Patient durch den vorher verabreichten Verdünner verblutet. Solche Wirkstoffe wurden zwar entwickelt, bisher zeigen sie jedoch alle unerwünschte Nebenwirkungen.
Zwei „Schnappschüsse“ zeigen die Funktionsweise des Rezeptors
„Wie der Rezeptor nach dem Schlüssel-Schloss-Prinzip genau funktioniert, war bislang noch nicht gut verstanden“, sagt Prof. Müller. „Dies ist jedoch eine wichtige Voraussetzung, um solch einen reversiblen, hochwirksamen und zugleich gut verträglichen, nebenwirkungsarmen Wirkstoff für die Unterbindung der Blutgerinnung zu entwickeln.“ In einem internationalen Team unter Federführung chinesischer Kollegen aus Shanghai und zusammen mit US-Forschern aus Bethesda und La Jolla ist es der Pharmazeutin gelungen, mit Hilfe der Röntgenstrukturanalyse zwei „Schnappschüsse“ des Rezeptors zu schießen: Einmal im „aufgeschlossenen“ Zustand, wenn ein geeigneter Bindungspartner für die Signalweiterleitung in das Blutplättchen sorgt. Die andere Aufnahme zeigt den P2Y12-Rezeptor im blockierten – „geschlossenen“ – Zustand. Diese Aufnahme wurde bereits in einer vorangegangenen „Nature“-Publikation online veröffentlicht.
Beide Publikationen werden in der gedruckten Ausgabe von „Nature“ unmittelbar aufeinanderfolgend erscheinen. „Anhand dieser beiden Bilder können wir nun nachvollziehen, wie sich der aus einem Protein bestehende Rezeptor beim Aufschließen verformt“, sagt Prof. Müller. Damit lassen sich auch Ansatzpunkte für die Entwicklung neuer Wirkstoffe finden, die selektiv und reversibel an den Rezeptor andocken.
„Allerdings ist noch weitere intensive Forschung notwendig, bis solche neuen Medikamente auf den Markt kommen“, sagt die Pharmazeutin der Universität Bonn. Da es viele Rezeptoren mit ganz ähnlichen Eigenschaften gibt, lässt die Erforschung des P2Y12-Rezeptors auf weitere Anwendungen hoffen. So ist der verwandte P2Y2-Rezeptor zum Beispiel an der Metastasierung von Tumorzellen beteiligt. „Auch hier könnten sich neue Optionen für die Krebsforschung ergeben“, blickt die Pharmazeutin optimistisch in die Zukunft.
Publikationen:
Agonist-bound structure of the human P2Y12 receptor, Fachjournal „Nature“, DOI: 10.1038/nature13288
Structure of the human P2Y12 receptor in complex with an antithrombotic drug, Fachjournal „Nature”, DOI: 10.1038/nature13083
Kontakt:
Prof. Dr. Christa E. Müller
Pharmazeutisches Institut
der Universität Bonn
Tel. 0228/732301
E-Mail: christa.mueller@uni-bonn.de
Hoffnung auf bessere Medikamente nach Schlaganfall Hoffnung auf bessere Medikamente nach Schlaganfall
Forscherteam unter Beteiligung der Uni Bonn entschlüsselt zentralen Rezeptor für die Blutgerinnung
Ein internationales Forscherteam unter Beteiligung der Universität Bonn hat zwei „Schnappschüsse“ eines Rezeptors aufgenommen, der für die Blutgerinnung von zentraler Bedeutung ist. Die Wissenschaftler hoffen nun, mit diesen Ergebnissen neuartige Medikamente entwickeln zu können. Dazu zählen maßgeschneiderte blutverdünnende Substanzen für Herzinfarkt- und Schlaganfallpatienten, deren Wirkung sich viel besser dosieren und auch wieder aufheben lässt. Die Forscher stellen ihre Ergebnisse im renommierten Fachjournal „Nature“ vor.

Prof. Dr. Christa E. Müller
- vom Pharmazeutischen Institut der Universität Bonn am Computerbildschirm, der links die schematische Darstellung einer Arterie mit Blutzellen und rechts die Röntgenstruktur des P2Y12-Rezeptors im Komplex mit dem Wirkstoff zeigt.
© Foto: Barbara Frommann/Uni Bonn
Alle Bilder in Originalgröße herunterladen
Der Abdruck im Zusammenhang mit der Nachricht ist kostenlos, dabei ist der angegebene Bildautor zu nennen.
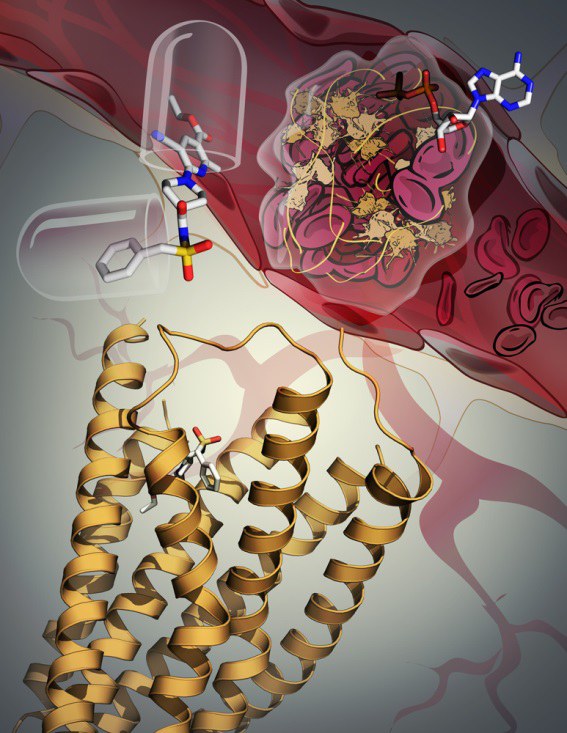
Kristallstruktur und Funktion des P2Y12-Rezeptors:
- Die Rezeptorstruktur ist als gelbes Band dargestellt. Der Ligand (oben rechts), der die Verklumpung des Blutes induziert, sowie der Wirkstoff, der die Blutplättchen-Aggregation hemmt (links oben), sind als farbige Stab-Molekülmodelle in einer Kapsel beziehungsweise auf einem Blutgerinnsel zu erkennen.
© Grafik: Katya Kadyshevskaya/Stevens Laboratory/The Scripps Research Institute


