Die Wissenschaftler der Universität Bonn, des Universitätsklinikums Bonn, des Life & Brain Centers und der TU Darmstadt wollen gemeinsam pharmakologische Werkzeuge entwickeln und einsetzen, um zu verstehen, auf welche Weise lebende Zellen miteinander kommunizieren. „Bei vielen Erkrankungen, zum Beispiel Krebs, ist diese zelluläre Kommunikation gestört“, sagt die Sprecherin der neuen DFG-Forschergruppe, Prof. Dr. Evi Kostenis vom Institut für pharmazeutische Biologie der Universität Bonn.
Zellen benutzen chemische Botenstoffe, wie zum Beispiel Hormone und Neurotransmitter, die auf Sensoren in der Zellmembran treffen und eine Reaktion der Zellen einleiten. Eine wichtige Rolle spielen dabei sogenannte G-Protein-gekoppelte Rezeptoren, die über G-Proteine chemische Signale an das Zellinnere weitergeben. „Genau diese G-Proteine wollen wir als Informationsübermittler pharmakologisch manipulieren“, sagt der stellvertretende Sprecher der Initiative, Prof. Dr. Klaus Mohr vom Pharmazeutischen Institut der Universität Bonn.
Bislang standen die G-Protein-gekoppelten Rezeptoren im Zentrum von Arzneimittelentwicklungen. Aber bei Lungenerkrankungen sowie bestimmten Schmerz- und Krebsformen kann dieses Konzept versagen, weil bei diesen Krankheiten gewöhnlich eine Vielzahl verschiedener Rezeptoren beteiligt ist. Mit einem Fokus auf G-Proteine ließe sich jedoch die krankhaft veränderte Rezeptorkommunikation konzertiert ausschalten. Genau auf diese G-Proteine, die erste Instanz in der Signalkette direkt unterhalb der G-Protein-gekoppelten Rezeptoren, richtet die Forschergruppe ihren Blick.
Die Wissenschaftler möchten zum einen die G-Proteine im Krankheitsgeschehen besser verstehen und sie gleichzeitig als neuen Ansatzpunkt für neuartige Therapien erforschen. „Derzeit stehen fast keine G-Protein-Blocker zur Verfügung“, sagt Prof. Kostenis. Mit geeigneten Hemmstoffen ließen sich jedoch absehbar Störsignale in der Kommunikation besser unterbinden. Dieses therapeutische Prinzip sollte sich nicht nur auf Krebserkrankungen, sondern auch auf Atemwegserkrankungen wie Asthma oder chronisch obstruktive Bronchitis anwenden lassen.
Aktuelle Studie in „Nature Communications“
Dass G-Proteine als Signalvermittler in der Tat ein vielversprechender Ansatzpunkt für pharmakologische Behandlungsverfahren sind, zeigte ein internationales Forscherteam unter Leitung von Prof. Kostenis, Prof. Dr. Thomas Tüting, und Prof. Dr. Gabriele König in einer aktuellen Studie, die kürzlich in „Nature Communications“ veröffentlicht wurde. Für den schwarzen Hautkrebs (malignes Melanom) entwickelte die Wissenschaftlergruppe eine neue therapeutische Strategie: Hemmung verschiedener G-Proteine zur effektiven Unterdrückung von Wachstum, Stoffwechsel und Beweglichkeit der entarteten Zellen.
Publikation: The experimental power of FR900359 to study Gq-regulated biological processes, Nature Communications, DOI: 10.1038/ncomms10156
Kontakt für die Medien:
Prof. Dr. Evi Kostenis
Institut für Pharmazeutische Biologie
Universität Bonn
Tel. 0170/2479037
E-Mail: kostenis@uni-bonn.de
Wie gestörte Zellkommunikation zu Krankheiten führt Wie gestörte Zellkommunikation zu Krankheiten führt
Deutsche Forschungsgemeinschaft (DFG) fördert Forschergruppe an der Uni Bonn mit 3,1 Millionen Euro
Forscher an der Universität Bonn untersuchen die Kommunikation von lebenden Zellen. Die Wissenschaftler möchten herausfinden, wie wirksam mit pharmakologischen Werkzeugen eingegriffen werden kann, wenn die Signalketten zwischen den Zellen gestört sind. Im Fokus des Teams stehen so genannte G-Proteine, die auch ein wichtiger Ansatzpunkt für die Entwicklung neuartiger Therapien sind. Die Deutsche Forschungsgemeinschaft (DFG) fördert die neue Forschergruppe in den nächsten drei Jahren mit 3,1 Millionen Euro.

Prof. Dr. Evi Kostenis
- vom Institut für Pharmazeutische Biologie der Universität Bonn.
© Foto: privat
Alle Bilder in Originalgröße herunterladen
Der Abdruck im Zusammenhang mit der Nachricht ist kostenlos, dabei ist der angegebene Bildautor zu nennen.
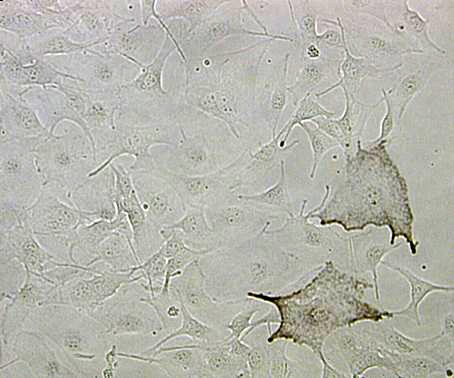
Durch die Zugabe des G-Protein-Hemmstoffs
- wird das Wachstum der Krebszellen gestoppt.
© Foto: Evelyn Gaffal/Thomas Tüting/UKB
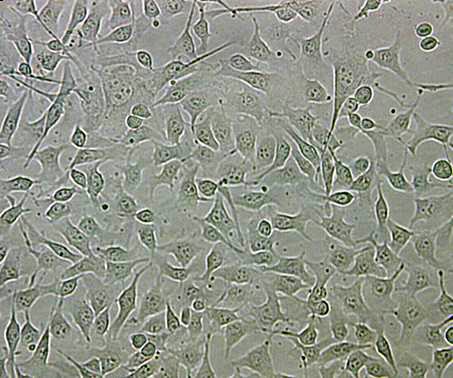
Schwarze Hautkrebszellen:
- Die bösartigen Zellen teilen sich stark.
© Foto: Evelyn Gaffal/Thomas Tüting/UKB


